
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Соңғы өзгертілген 2025-01-22 17:03.
The түзілу энтальпиясы үшін элемент өзінің элементтік күйінде әрқашан болады 0 өйткені табиғи қосылыс түзу үшін энергия қажет емес. Зат болған кезде қалыптасты оның ең тұрақты түрінен элементтері , өзгеріс энтальпия орын алады.
Сол сияқты, қандай заттардың түзілу энтальпиясы нөлге тең?
Барлық элементтер стандартты күйде (оттегі газы, қатты көміртек түрінде графит , т.б.) нөлдің стандартты түзілу энтальпиясы бар, өйткені олардың түзілуіне ешқандай өзгеріс қатыспайды.
Бұдан кейін судың пайда болу энтальпиясы қандай деген сұрақ туындайды? Термохимиялық желінің 1.118 нұсқасы негізінде таңдалған ATcT түзілу энтальпиясы
| Түр атауы | Формула | ΔfH°(298,15 К) |
|---|---|---|
| Су | H2O (кр, экв.пресс.) | -292.740 |
Тиісінше, алмаз элемент болғанымен стандартты түзілу энтальпиясы неге нөлге тең емес?
The түзілудің стандартты энтальпиясы үшін элемент оның ішінде стандартты мемлекет болып табылады НӨЛ !!!! Сонымен, C (s, графит) үшін ΔH°f нөл , бірақ C (s,) үшін ΔH°f алмаз ) 2 кДж/моль. Себебі графит - бұл стандартты көміртегі күйі, гауһар емес.
Delta h нөлге тең болғанда бұл нені білдіреді?
Олар энтальпиядағы өзгерістерді ғана өлшей алады. Энтальпия оң болғанда және дельта H -дан үлкен нөл , бұл білдіреді жүйе жылуды сіңіреді. Бұл эндотермиялық реакция деп аталады. Энтальпия теріс болғанда және дельта H -ден аз нөл , бұл білдіреді жүйе жылуды бөледі. Бұл экзотермиялық реакция деп аталады.
Ұсынылған:
Неліктен магнит ағыны максималды болғанда индукцияланған ЭҚК нөлге тең болады?

Катушка тік тұрған кезде магнит ағынында ешқандай өзгеріс болмайды (яғни эмф=0), себебі катушкалар өріс сызықтарын «кесіп өтпейді». Катушкалар өріс сызықтарына перпендикуляр болған кезде индукцияланған ЭҚК нөлге тең, ал параллель болғанда максимум. Есіңізде болсын, индукцияланған ЭҚК - бұл магнит ағынының байланысының өзгеру жылдамдығы
Неліктен катушка магниттің дәл ортасынан өткенде ЭҚК нөлге тең?
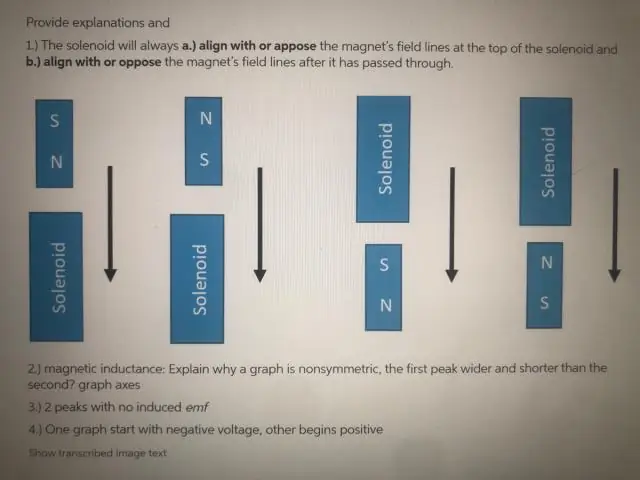
ЭҚК бір сәтке тек нөлге тең, өйткені магнит катушканың дәл ортасынан өтеді. Себебі магниттің бір ұшындағы N полюсінің катушканың сол ұшына әсері магниттің S полюсінің катушканың екінші ұшына әсерімен дәл жойылады
Као түзілу энтальпиясы неге тең?

Түзілетін қосылыс жылуларының кестесі ΔHf (кДж/моль) CaCO3 -1207,0 CaO(s) -635,5 Ca(OH)2(s) -986,6 CaSO4(s) -1432,7
Қай процесте орындалған жұмыс нөлге тең?

Изохоралық процесс (тұрақты көлем) Изохоралық процесс - бұл көлем тұрақты болып қалатын процесс, яғни жүйенің атқаратын жұмысы нөлге тең болады. Изохоралық процесс изометриялық процесс немесе изоволюметриялық процесс деп те аталады
Жердегі элементтердің көптігі адамдардағы элементтердің көптігімен қалай салыстырылады?

Оттегі - жер бетінде де, адамдарда да ең көп таралған элемент. Адамдарда органикалық қосылыстар түзетін элементтердің көптігі артады, ал жер бетінде металлоидтардың көптігі артады. Жер бетінде көп кездесетін элементтер тіршілікті қамтамасыз ету үшін өте маңызды
