
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Соңғы өзгертілген 2025-01-22 17:03.
Niels Бор түсіндірді the сызықтық спектр сутегі атом электрон дөңгелек орбиталарда қозғалды және тек белгілі бір радиустары бар орбиталарға рұқсат етілген деп есептей отырып. Ядроға ең жақын орбита оның негізгі күйін көрсетті атом және ең тұрақты болды; одан да алыс орбиталар жоғары энергиялы қоздырылған күйлер болды.
Сол сияқты Бор моделі нені түсіндіреді?
The Бор моделі атомдардағы электрондардың ядроның айналасында энергиясы әртүрлі орбиталарда болатынын көрсетеді (күнді айналатын планеталарды елестетіңіз). Бор әртүрлі энергияның осы орбиталарын сипаттау үшін энергия деңгейлері (немесе қабықтар) терминін пайдаланды.
Сонымен қатар, Бор үлгісін қалай оқисыз?
- Ядро сызыңыз.
- Ядродағы нейтрондар мен протондар санын жаз.
- Бірінші энергия деңгейін сызыңыз.
- Төмендегі ережелерге сәйкес энергия деңгейлеріндегі электрондарды салыңыз.
- Әр деңгейге қанша электрон салынғанын және пайдаланылатын электрондардың санын қадағалаңыз.
Сол сияқты, атомдық спектрлер қалай жасалады?
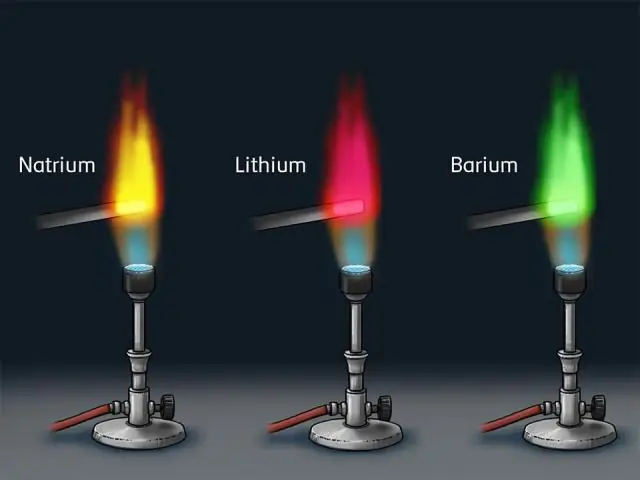
Қашан атомдар қозғалған кезде олар әртүрлі түстерге сәйкес келетін белгілі бір толқын ұзындығындағы жарық шығарады. Шығарылатын жарықты арасында қараңғы бос орындар бар түрлі-түсті сызықтар қатары ретінде байқауға болады; бұл түсті сызықтар қатары сызық немесе деп аталады атомдық спектрлер . Әрбір элемент өндіреді бірегей жиынтығы спектрлік сызықтар.
Бор өз моделінде сутегінің сызықтық спектрін түсіндіру үшін қандай қорытынды жасады?
Түсініктеме: Бор бұл болжамды тек аз ғана екендігіне негіздеді сызықтар ішінде спектр -ның сутегі атом және ол сенді сызықтар атомдағы электронның бір орбитадан екінші орбитаға ауысуы кезінде жарықтың бөлінуінің немесе жұтылуының нәтижесі болды.
Ұсынылған:
Нил Бор атом моделі дегеніміз не?

Нильс Бор 1915 жылы атомның Бор моделін ұсынды. Бор моделі теріс зарядталған электрондар күнді айналатын планеталарға ұқсас шағын, оң зарядталған ядроны айналатын планеталық модель (орбиталардың жазық емес екендігін қоспағанда)
Резерфордтың атом моделі қалай аталады?

Резерфордтың атом моделі ядролық модель деп аталды. Ядролық атомда атомның барлық дерлік массасын құрайтын протондар мен нейтрондар атомның ортасында ядрода орналасқан. Электрондар ядроның айналасында таралады және атом көлемінің көп бөлігін алады
Шредингер моделі Бор моделінен несімен ерекшеленеді?

Бор моделінде электрон ядроның айналасындағы қозғалмайтын орбиталарда бөлшек ретінде қарастырылады. Шредингер үлгісі (Кванттық механикалық модель) электронның үш өлшемді кеңістікті алуына мүмкіндік берді. Сондықтан атомдағы электрондардың таралуын сипаттау үшін үш координат немесе үш кванттық сандар қажет болды
Неліктен Бор моделін атомның планетарлық моделі деп атауға болады?

Оның «планетарлық модель» деп аталу себебі, электрондар ядроны айналып қозғалады, планеталар Күнді айнала қозғалатын сияқты (бұдан басқа планеталар тартылыс күшінің әсерінен Күннің жанында, ал электрондар ядроның жанында деп аталатын нәрсе арқылы ұсталады. Кулон күші)
Нильс Бор өзінің атомдық моделінде электрондарды қалай сипаттады?
Бор атомдық моделі: 1913 жылы Бор электрондардың ядро айналасында тұрақты орбиталарға ие болуын түсіндіру үшін атомның квантталған қабықша моделін ұсынды. Электронның энергиясы орбитаның өлшеміне байланысты және кішірек орбиталар үшін төмен. Сәулелену электрон бір орбитадан екіншісіне секіргенде ғана пайда болуы мүмкін
