
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:38.
- Соңғы өзгертілген 2025-01-22 17:03.
Авогадро заңы газдың моль саны мен оның арасында тікелей байланыс бар екенін көрсетеді көлемі . Мұны да көрсетуге болады қолдану теңдеу: V1/n1 = V2/n2. Егер моль саны екі еселенсе, онда көлемі еселенеді.
Осылайша Авогадро заңының формуласы қандай?
Авогадро заңының формуласы Мұндағы «V» газдың көлемі, «n» газ мөлшері (газ мольдерінің саны) және «k» берілген қысым мен температура үшін тұрақты шама. Ақиқатында, Авогадро заңы , оның қойған гипотеза, арасында болды заңдар Идеал газ Заң негізделген.
Сонымен қатар, Авогадро заңының мысалы қандай? Авогадро заңы газдың көлемі газдың моль санына тура пропорционал екенін айтады. Міне, кейбіреулер мысалдар . Баскетбол добын жарып жатқанда, оған көбірек газ молекулалары түседі. Молекулалар неғұрлым көп болса, соғұрлым көлем көп болады. Екі шарда бірдей молекулалар бар.
Оның үстіне Авогадро заңы нені көрсетеді бұл зертхана заңды дәлелдейді Сіз қайдан білесіз?
Заманауи мәлімдеме болып табылады : Авогадро заңы «барлық газдардың бірдей көлемдерінде, бірдей температура мен қысымда молекулалар саны бірдей» деп тұжырымдайды. Берілген a массасы үшін идеал газ , газдың көлемі мен мөлшері (моль). болып табылады температура мен қысымға тура пропорционал болып табылады тұрақты.
Авогадро гипотезасы бойынша көлемдерді біріктіру заңы қалай түсіндіріледі?
(а) Көлемдерді біріктіру заңы бойынша Авогадро гипотезасы : Құрамында бірдей газдар бар томдар температура мен қысымның бірдей сыртқы жағдайларында молекулалар саны бірдей болады. Бұл газ молекулалары кіші бүтін сандардың қатынасында әрекеттеседі, сондықтан олардың (газ) томдар сонымен қатар кіші бүтін сандардың қатынасында болады.
Ұсынылған:
4-сыныпта көлемді қалай табуға болады?

Көлем – тұтас фигураны құрайтын текше бірліктердің саны. Төменде әртүрлі қатты фигура түрлері көрсетілген. Тік бұрышты призманың көлемін текше бірліктердің санын санау немесе формуланы қолдану арқылы табуға болады. Тік бұрышты призманың көлемін табу формуласы V = l x w x h
7-сыныпта көлемді қалай табуға болады?
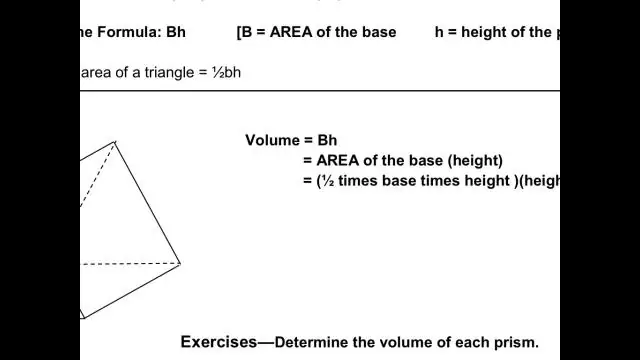
Көлем текше бірлікпен көрсетіледі. 7-сыныпта жиі оқытылатын көлемдер: Текше Қабырғаның ұзындығын өзіне үш есе көбейту; формуласы A = l^3. Тік бұрышты призма Үш жақтың ұзындықтарын (ұзындығы, ені және биіктігі) бір-бірімен көбейтіңіз: A = lwh
ДНҚ концентрациясын сіңіру арқылы қалай табуға болады?

ДНҚ концентрациясы абсорбентті 260 нм-де өлшеу, A260 өлшемін бұлдырлық үшін реттеу (320 нм-де сіңіру арқылы өлшенеді), сұйылту коэффициентіне көбейту және A260 1,0 = 50 мкг/мл таза dsDNA деген қатынасты пайдалану арқылы бағаланады
Көлемді текше бірлікте қалай табуға болады?

Өлшем бірліктері Көлем = ұзындық x ені x биіктік. Текшенің көлемін анықтау үшін тек бір жағын білу керек. Көлемнің өлшем бірліктері текше бірлік болып табылады. Көлемі үш өлшемді. Қабырғаларды кез келген ретпен көбейтуге болады. Ұзындығы, ені немесе биіктігінің қай жағын атайтыныңыз маңызды емес
Авогадро заңы қалай қолданылады?

Авогадро заңы газдың көлемі газдың мольдерінің санына тура пропорционал екенін айтады. Баскетбол добын жарып жатқанда, оған көбірек газ молекулалары түседі. Молекулалар неғұрлым көп болса, соғұрлым көлем көп болады. Баскетбол добы үрлейді
